帕金森病(Parkinson’s disease, PD)是因中脑黑质致密部区域多巴胺能神经元变性及丢失引起的老年神经退行性疾病。已有临床试验表明移植胎儿腹侧中脑组织(fetal ventral mesencephalon, fVM)可以补充脑内丢失的多巴胺能神经元,在一些帕金森病患者中能观测到一定疗效。但fVM移植治疗PD仍然存在一些亟待解决的,比如伦理、异质性以及可移植组织供量不足等问题。
陈志国教授团队采用三维立体培养方式,诱导人源多能干细胞生成一种与fVM具有高度相似性的细胞组织——中脑类器官(human midbrain organoids, hMOs),为这一领域的研究提供了一个新的视角,或将打破上述fVM移植所面临的困境。
该研究成果发表在生物医学1区期刊《Theranostics》(IF: 11.600),题为“Human iPSC-derived midbrain organoids functionally integrate into striatum circuits and restore motor function in a mouse model of Parkinson’s disease”。

fVM组织主要由非神经元细胞组成,如星形胶质细胞、小胶质细胞和内皮细胞;神经元仅占总细胞群的5.6%。在这一小部分神经元中,约70%为多巴胺能神经元谱系,30%为GABA能神经元,2-3%为谷氨酰胺能神经元。这些细胞会引起运动障碍等严重副作用。在本研究中,hMOs培养至第15天时未检测到星形胶质细胞、少突胶质细胞、GABA能神经元、谷氨酰胺能或5-羟色胺能神经元。而且,在发育过程中未检测到与5-羟色胺能细胞相关的基因表达。这些结果表明,hMO比fVM具有更均匀的细胞性质。
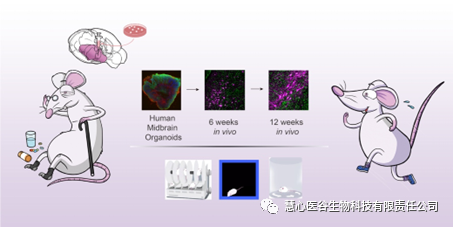
在此项研究中,陈志国教授团队使用三维立体培养方式,诱导人源多能干细胞生成hMOs,并通过颅内立体定位注射方式将其移植至PD小鼠脑内纹状体。hMOs在宿主脑内能继续成熟为多巴胺能神经元,并随着在脑内时间的延长而逐渐改善小鼠运动功能障碍。hMOs神经元轴突能在宿主中枢神经系统内延伸并与宿主神经元发生整合。此外,截止至实验终点,接受hMOs移植的小鼠体内未见明显肿瘤形成。上述实验结果提示,hMOs治疗帕金森病临床前研究展现了其安全性及有效性,为临床细胞治疗提供一种新的思路。
原文链接
https://www.thno.org/v13p2673
Copyright © 北京慧心医谷生物科技有限责任公司